マイクロチップの新技術による超並列デジタルバイオ計測:医療機器ニュース
東京大学は、標的物質の濃度勾配を形成する機構を実装するマイクロ流路を内蔵したチップを開発することで、デジタルバイオ計測の超並列化に成功した。
東京大学は2018年8月10日、標的物質の濃度勾配を形成する機構を実装するマイクロ流路を内蔵したチップを開発することで、デジタルバイオ計測の超並列化を可能にしたと発表した。同大学大学院工学系研究科 講師の渡邉力也氏らの研究グループによる成果だ。
デジタルバイオ計測は、数万個以上の微小な試験管を集積したマイクロチップを活用し、単一の生体分子から機能や物性を高感度かつ定量的に計測する手法だ。デジタルバイオ計測に利用するマイクロチップは試験管を集積するが、小型のため、それらを並列利用することは困難で、スループットの向上が難しいという課題があった。
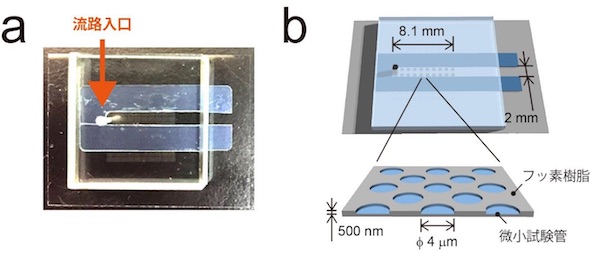
研究グループは、標的物質の濃度勾配を形成する機構をマイクロチップに実装し、チップ上の各試験管に異なる組成の溶液を数秒間で封入する技術を開発。まず、これまで利用されてきたマイクロチップ(24×32mm)上に、直線の流路(幅:2mm、高さ:0.3mm)を設置した。マイクロチップには、容積が数フェムトリットル(フェムトは1000兆分の1)程度の均一な微小試験管を約10万個集積している。
この流路を標的物質を含む水溶液で満たした後、任意の容量の希釈液を一定の流速で導入すると、流路内の標的物質は移流拡散プロセスによって希釈され、流れ方向に沿って一直線に濃度勾配が流路の底面に形成される。微小試験管は流路の底面にあるため、流路内の濃度勾配に沿って、各試験管に含まれる標的物質の濃度も定量的に変化させることが可能だ。最後に、濃度勾配を形成した後すぐに脂質溶液を流路へ導入し、各試験管の開口部に人工生体膜でふたをする。
この方法では、流路に導入する希釈液の容量や流速を制御することにより、チップ上の各試験管に封入する標的物質の濃度を10〜1000倍程度の範囲で連続的に変化させることができる。従来のプレートリーダー法とは異なり、1種類の希釈液を数秒間導入するだけで、異なる組成の水溶液を試験管に封入できる。また、1本の流路と電動ピペットで実験が可能で、分析装置への実装の際にコスト削減が期待できる。
研究グループは、このマイクロチップを用いて、従来不可能だった試験管の並列利用による「デジタルバイオ計測のハイスループット化(超並列化)」に成功。具体的には、まずマイクロチップ上の各試験管に、酵素などの1分子の標的生体分子と任意の濃度の基質を封入する。その後、生体分子による基質の分解反応に伴い、試験管の中に反応生成物が蓄積し、濃縮される。生体分子の反応に伴って蛍光を発する基質を利用すると、蛍光強度の増加速度から生体分子の反応速度を定量的に測定できる。
実際に、従来のバイオセンサーに汎用されてきた酵素(ALP)に対して、1枚のマイクロチップから、さまざまな基質濃度での反応速度を並列測定することに成功した。これにより、基質の結合速度定数などの酵素の基礎データを容易に取得できる。生体膜を各試験管に実装するため、市販薬の主な標的である「膜タンパク質」でのデジタルバイオ計測の超並列化にも応用できることも実証した。
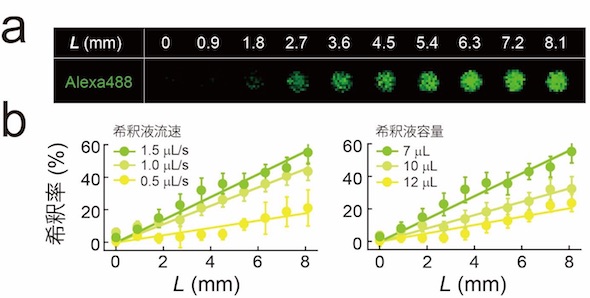 マイクロチップ上での標的物質の濃度勾配の形成。(a)流路の入口からの距離と微小試験管に封入された標的物質(緑色蛍光色素:Alexa488)の蛍光画像。(b)流路の入口からの距離と試験管に封入される標的物質の希釈率の関係。(クリックで拡大) 出典:東京大学
マイクロチップ上での標的物質の濃度勾配の形成。(a)流路の入口からの距離と微小試験管に封入された標的物質(緑色蛍光色素:Alexa488)の蛍光画像。(b)流路の入口からの距離と試験管に封入される標的物質の希釈率の関係。(クリックで拡大) 出典:東京大学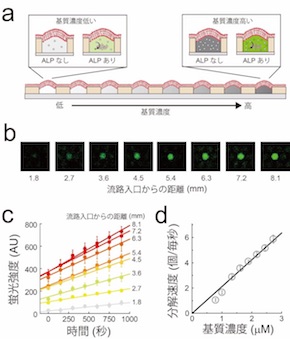 ALPを標的とした超並列バイオ計測。(a)ALPを標的とした超並列バイオ計測の模式図。(b, c)計測開始から15分後の試験管の蛍光画像と蛍光強度の経時変化。(d)封入した基質濃度とALPの加水分解速度の相関計測結果。(クリックで拡大) 出典:東京大学
ALPを標的とした超並列バイオ計測。(a)ALPを標的とした超並列バイオ計測の模式図。(b, c)計測開始から15分後の試験管の蛍光画像と蛍光強度の経時変化。(d)封入した基質濃度とALPの加水分解速度の相関計測結果。(クリックで拡大) 出典:東京大学関連記事
 心臓での抗がん剤の副作用を再現、微細加工技術応用のマイクロ流体デバイスで
心臓での抗がん剤の副作用を再現、微細加工技術応用のマイクロ流体デバイスで
京都大学は、微細加工技術を駆使した生体外ヒトモデル「Body on a Chip」の開発に成功した。患者や健常者、実験動物などに頼ることなく、薬の効能・効果や毒性を評価できる。 ショット、マイクロ流体チップなどに用いるバイオ向けガラス基板の販売を強化
ショット、マイクロ流体チップなどに用いるバイオ向けガラス基板の販売を強化
SCHOTT(ショット)は、成長著しい医療や生命科学の分野向けに、特性や厚さの異なるさまざまなガラス基板を取りそろえている。独自のマイクロレーザー構造化技術を用いてガラス基板を加工し、直径30μmの構造物を作ることが可能だ。 マイクロ流体チップのパッケージングに新手法、従来と逆で「付けてから貼る」
マイクロ流体チップのパッケージングに新手法、従来と逆で「付けてから貼る」
理化学研究所は、細胞や生体分子の機能を損なわずに、マイクロ流体チップ中にパッケージングする手法を開発した。ガラス板に細胞や生体分子を所定位置に定着させた後、ガラス板を常温での表面処理と加圧で貼り合わせて流路を形成する。 失明を招く加齢黄斑変性の病態を生体組織チップ上で一部再現、東北大学
失明を招く加齢黄斑変性の病態を生体組織チップ上で一部再現、東北大学
東北大学は、失明につながる網膜疾患の病態の一部を生体組織チップ上で再現することに成功した。疾患モデル動物の代替として、病態解析や創薬スクリーニングに応用できる可能性がある。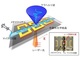 バイオケミカルセンサーチップを開発、微量の液体から特定の溶質を高感度に検出
バイオケミカルセンサーチップを開発、微量の液体から特定の溶質を高感度に検出
大阪大学は、レーザー光の照射により非線形光学結晶から発生するテラヘルツ波を用いて、極微量の溶液中の溶質濃度を高感度かつ定量的に検出できる超高感度バイオケミカルセンサーチップを開発した。
関連リンク
Copyright © ITmedia, Inc. All Rights Reserved.
医療機器の記事ランキング
- 医薬品向け製造、品質管理システムのサプスクリプション型サービスを開始
- 画像診断支援AI技術の開発を支援するクラウドサービスの提供を開始
- トウモロコシ由来のオリゴペプチドが肥満や脂肪肝を改善する
- 3ステップ約3分で40種類の薬物を尿から検出する手法を開発
- 内視鏡システムのクラウド化に関する実証実験を開始
- 骨再生材料であるリン酸八カルシウムの量産化に成功
- 医療機器よりも難題!? Non-SaMDに影響が及ぶ米国のIoTセキュリティ政策
- AIを活用して慢性腰痛のヘルスケアを支援する技術を開発
- 米国病院は新型コロナの院内クラスター対策にDXを導入、働き方改革も進める
- オリンパスが八王子に本社を移転、全ての事業機能を集約したグローバル本社へ